Aunque todos los átomos del mismo elemento contienen el mismo número de protones, su número de neutrones puede variar. Saber cuántos neutrones hay en un átomo en particular puede ayudarte a determinar si se trata de un átomo regular de ese elemento o un isótopo, que tendrá neutrones adicionales o menos.[1] Determinar el número de neutrones en un átomo es bastante simple y no requiere experimentación. Para calcular la cantidad de neutrones en un átomo regular o un isótopo, todo lo que tiene que hacer es seguir estas instrucciones con una tabla periódica en mano.
Método uno de dos:
Encontrar el número de neutrones en un átomo regular
-
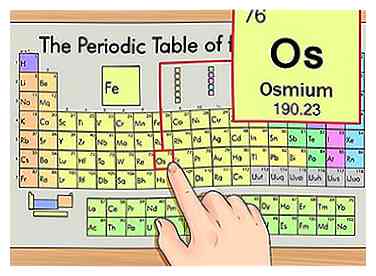 1 Ubique el elemento en la tabla periódica. Para este ejemplo, veremos osmio (Os), que está en la sexta fila hacia abajo.
1 Ubique el elemento en la tabla periódica. Para este ejemplo, veremos osmio (Os), que está en la sexta fila hacia abajo. -
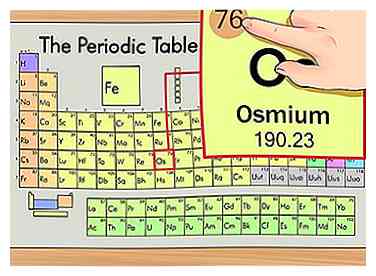 2 Encuentra el número atómico del elemento. Este tiende a ser el número más visible perteneciente a un elemento dado y generalmente se encuentra sobre el símbolo del elemento, ya sea en el medio del cuadro o en la esquina superior izquierda. (En la tabla que estamos usando, de hecho, no se enumeran otros números). El número atómico es la cantidad de protones en un solo átomo de ese elemento. Os es el número 76, lo que significa que un átomo de osmio tiene 76 protones.
2 Encuentra el número atómico del elemento. Este tiende a ser el número más visible perteneciente a un elemento dado y generalmente se encuentra sobre el símbolo del elemento, ya sea en el medio del cuadro o en la esquina superior izquierda. (En la tabla que estamos usando, de hecho, no se enumeran otros números). El número atómico es la cantidad de protones en un solo átomo de ese elemento. Os es el número 76, lo que significa que un átomo de osmio tiene 76 protones. - El número de protones nunca cambia en un elemento; Básicamente es lo que hace que ese elemento ese elemento.
-
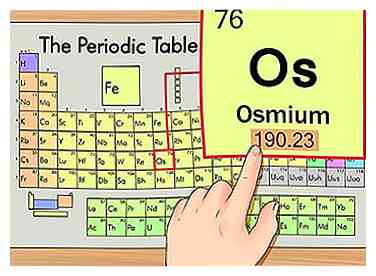 3 Encuentra el peso atómico del elemento. Este número generalmente se encuentra debajo del símbolo atómico. Tenga en cuenta que la tabla en este ejemplo se basa únicamente en el número atómico y no enumera el peso atómico. Por lo general, este no siempre será el caso. El osmio tiene un peso atómico de 190.23.
3 Encuentra el peso atómico del elemento. Este número generalmente se encuentra debajo del símbolo atómico. Tenga en cuenta que la tabla en este ejemplo se basa únicamente en el número atómico y no enumera el peso atómico. Por lo general, este no siempre será el caso. El osmio tiene un peso atómico de 190.23. -
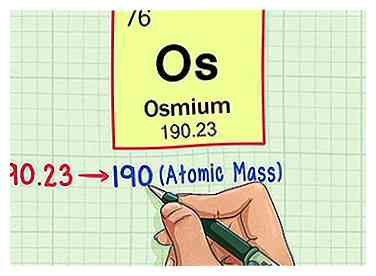 4 Redondee el peso atómico al número entero más cercano para encontrar la masa atómica. En nuestro ejemplo, 190.23 se redondearía a 190, lo que daría como resultado una masa atómica de 190 para el osmio.
4 Redondee el peso atómico al número entero más cercano para encontrar la masa atómica. En nuestro ejemplo, 190.23 se redondearía a 190, lo que daría como resultado una masa atómica de 190 para el osmio. - El peso atómico es un promedio de los isótopos del elemento, por eso no suele ser un número entero.
-
 5 Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se compone de sus protones y neutrones, restar la cantidad de protones (es decir, el número atómico) de la masa atómica le dará la calculado cantidad de neutrones en el átomo Los números después del punto decimal representan la masa generalmente muy pequeña de los electrones en el átomo. En nuestro ejemplo, esto es: 190 (peso atómico) - 76 (número de protones) = 114 (número de neutrones).
5 Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se compone de sus protones y neutrones, restar la cantidad de protones (es decir, el número atómico) de la masa atómica le dará la calculado cantidad de neutrones en el átomo Los números después del punto decimal representan la masa generalmente muy pequeña de los electrones en el átomo. En nuestro ejemplo, esto es: 190 (peso atómico) - 76 (número de protones) = 114 (número de neutrones). -
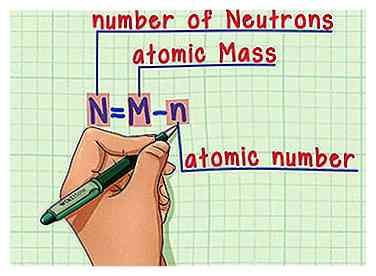 6 Recuerde la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula:
6 Recuerde la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula: - N = M - n
- N = número de norteEutrons
- M = atómico METROculo
- n = atómico norteocre oscuro
- N = M - n
Método dos de dos:
Encontrar el número de neutrones en un isótopo
-
 1 Ubique el elemento en la tabla periódica. Como ejemplo, veremos el isótopo de carbono-14. Dado que la forma no isotópica de carbono-14 es simplemente carbono (C), encuentre carbono en la tabla periódica (en la segunda fila hacia abajo).
1 Ubique el elemento en la tabla periódica. Como ejemplo, veremos el isótopo de carbono-14. Dado que la forma no isotópica de carbono-14 es simplemente carbono (C), encuentre carbono en la tabla periódica (en la segunda fila hacia abajo). -
 2 Encuentra el número atómico del elemento. Este tiende a ser el número más visible perteneciente a un elemento dado y generalmente se encuentra sobre el símbolo del elemento. (En nuestro gráfico de ejemplo, de hecho, no se enumeran otros números). El número atómico es la cantidad de protones en un solo átomo de ese elemento. C es el número 6, lo que significa que un átomo de carbono tiene 6 protones.
2 Encuentra el número atómico del elemento. Este tiende a ser el número más visible perteneciente a un elemento dado y generalmente se encuentra sobre el símbolo del elemento. (En nuestro gráfico de ejemplo, de hecho, no se enumeran otros números). El número atómico es la cantidad de protones en un solo átomo de ese elemento. C es el número 6, lo que significa que un átomo de carbono tiene 6 protones. -
 3 Encuentra la masa atómica. Esto es increíblemente fácil con los isótopos, ya que se nombran según su masa atómica. El carbono 14, por ejemplo, tiene una masa atómica de 14. Una vez que encuentras la masa atómica del isótopo, el proceso es el mismo que para encontrar el número de neutrones en un átomo regular.
3 Encuentra la masa atómica. Esto es increíblemente fácil con los isótopos, ya que se nombran según su masa atómica. El carbono 14, por ejemplo, tiene una masa atómica de 14. Una vez que encuentras la masa atómica del isótopo, el proceso es el mismo que para encontrar el número de neutrones en un átomo regular. -
 4 Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se encuentra con sus protones y neutrones, restar la cantidad de protones (es decir, el número atómico) de la masa atómica le dará el calculado cantidad de neutrones en el átomo En nuestro ejemplo, esto es: 14 (masa atómica) - 6 (número de protones) = 8 (número de neutrones).
4 Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se encuentra con sus protones y neutrones, restar la cantidad de protones (es decir, el número atómico) de la masa atómica le dará el calculado cantidad de neutrones en el átomo En nuestro ejemplo, esto es: 14 (masa atómica) - 6 (número de protones) = 8 (número de neutrones). -
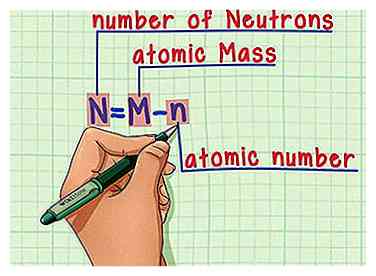 5 Recuerde la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula:
5 Recuerde la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula: - N = M - n
- N = número de norteEutrons
- M = atómico METROculo
- n = atómico norteocre oscuro
- N = M - n
Facebook
Twitter
Google+
 Minotauromaquia
Minotauromaquia
 1 Ubique el elemento en la tabla periódica. Para este ejemplo, veremos osmio (Os), que está en la sexta fila hacia abajo.
1 Ubique el elemento en la tabla periódica. Para este ejemplo, veremos osmio (Os), que está en la sexta fila hacia abajo.  2 Encuentra el número atómico del elemento. Este tiende a ser el número más visible perteneciente a un elemento dado y generalmente se encuentra sobre el símbolo del elemento, ya sea en el medio del cuadro o en la esquina superior izquierda. (En la tabla que estamos usando, de hecho, no se enumeran otros números). El número atómico es la cantidad de protones en un solo átomo de ese elemento. Os es el número 76, lo que significa que un átomo de osmio tiene 76 protones.
2 Encuentra el número atómico del elemento. Este tiende a ser el número más visible perteneciente a un elemento dado y generalmente se encuentra sobre el símbolo del elemento, ya sea en el medio del cuadro o en la esquina superior izquierda. (En la tabla que estamos usando, de hecho, no se enumeran otros números). El número atómico es la cantidad de protones en un solo átomo de ese elemento. Os es el número 76, lo que significa que un átomo de osmio tiene 76 protones.  3 Encuentra el peso atómico del elemento. Este número generalmente se encuentra debajo del símbolo atómico. Tenga en cuenta que la tabla en este ejemplo se basa únicamente en el número atómico y no enumera el peso atómico. Por lo general, este no siempre será el caso. El osmio tiene un peso atómico de 190.23.
3 Encuentra el peso atómico del elemento. Este número generalmente se encuentra debajo del símbolo atómico. Tenga en cuenta que la tabla en este ejemplo se basa únicamente en el número atómico y no enumera el peso atómico. Por lo general, este no siempre será el caso. El osmio tiene un peso atómico de 190.23.  4 Redondee el peso atómico al número entero más cercano para encontrar la masa atómica. En nuestro ejemplo, 190.23 se redondearía a 190, lo que daría como resultado una masa atómica de 190 para el osmio.
4 Redondee el peso atómico al número entero más cercano para encontrar la masa atómica. En nuestro ejemplo, 190.23 se redondearía a 190, lo que daría como resultado una masa atómica de 190 para el osmio.  5 Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se compone de sus protones y neutrones, restar la cantidad de protones (es decir, el número atómico) de la masa atómica le dará la calculado cantidad de neutrones en el átomo Los números después del punto decimal representan la masa generalmente muy pequeña de los electrones en el átomo. En nuestro ejemplo, esto es: 190 (peso atómico) - 76 (número de protones) = 114 (número de neutrones).
5 Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se compone de sus protones y neutrones, restar la cantidad de protones (es decir, el número atómico) de la masa atómica le dará la calculado cantidad de neutrones en el átomo Los números después del punto decimal representan la masa generalmente muy pequeña de los electrones en el átomo. En nuestro ejemplo, esto es: 190 (peso atómico) - 76 (número de protones) = 114 (número de neutrones).  6 Recuerde la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula:
6 Recuerde la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula:  1 Ubique el elemento en la tabla periódica. Como ejemplo, veremos el isótopo de carbono-14. Dado que la forma no isotópica de carbono-14 es simplemente carbono (C), encuentre carbono en la tabla periódica (en la segunda fila hacia abajo).
1 Ubique el elemento en la tabla periódica. Como ejemplo, veremos el isótopo de carbono-14. Dado que la forma no isotópica de carbono-14 es simplemente carbono (C), encuentre carbono en la tabla periódica (en la segunda fila hacia abajo).  2 Encuentra el número atómico del elemento. Este tiende a ser el número más visible perteneciente a un elemento dado y generalmente se encuentra sobre el símbolo del elemento. (En nuestro gráfico de ejemplo, de hecho, no se enumeran otros números). El número atómico es la cantidad de protones en un solo átomo de ese elemento. C es el número 6, lo que significa que un átomo de carbono tiene 6 protones.
2 Encuentra el número atómico del elemento. Este tiende a ser el número más visible perteneciente a un elemento dado y generalmente se encuentra sobre el símbolo del elemento. (En nuestro gráfico de ejemplo, de hecho, no se enumeran otros números). El número atómico es la cantidad de protones en un solo átomo de ese elemento. C es el número 6, lo que significa que un átomo de carbono tiene 6 protones.  3 Encuentra la masa atómica. Esto es increíblemente fácil con los isótopos, ya que se nombran según su masa atómica. El carbono 14, por ejemplo, tiene una masa atómica de 14. Una vez que encuentras la masa atómica del isótopo, el proceso es el mismo que para encontrar el número de neutrones en un átomo regular.
3 Encuentra la masa atómica. Esto es increíblemente fácil con los isótopos, ya que se nombran según su masa atómica. El carbono 14, por ejemplo, tiene una masa atómica de 14. Una vez que encuentras la masa atómica del isótopo, el proceso es el mismo que para encontrar el número de neutrones en un átomo regular.  4 Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se encuentra con sus protones y neutrones, restar la cantidad de protones (es decir, el número atómico) de la masa atómica le dará el calculado cantidad de neutrones en el átomo En nuestro ejemplo, esto es: 14 (masa atómica) - 6 (número de protones) = 8 (número de neutrones).
4 Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se encuentra con sus protones y neutrones, restar la cantidad de protones (es decir, el número atómico) de la masa atómica le dará el calculado cantidad de neutrones en el átomo En nuestro ejemplo, esto es: 14 (masa atómica) - 6 (número de protones) = 8 (número de neutrones).  5 Recuerde la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula:
5 Recuerde la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula: