Encontrar la cantidad de protones, neutrones y electrones en un elemento dado no es tan difícil como parece. Muchas veces, parte de tu respuesta estará frente a ti en la tabla periódica. Una vez que sepa dónde buscar, encontrar la cantidad de protones, neutrones y electrones será muy fácil.
Parte uno de dos:
Cálculo de protones, electrones y neutrones
-
 1 Obtenga una tabla periódica de elementos. La tabla periódica es una tabla que organiza elementos por su estructura atómica. Está codificado por colores y le asigna a cada elemento una abreviatura única de 1 o 2 letras. Otra información elemental incluye el peso atómico y el número atómico.[1]
1 Obtenga una tabla periódica de elementos. La tabla periódica es una tabla que organiza elementos por su estructura atómica. Está codificado por colores y le asigna a cada elemento una abreviatura única de 1 o 2 letras. Otra información elemental incluye el peso atómico y el número atómico.[1] - Puede encontrar una tabla periódica en línea o en un libro de química.
- En las pruebas, normalmente, se proporcionará una tabla periódica.
-
 2 Encuentra tu elemento en la tabla periódica. La tabla ordena elementos por número atómico y los separa en tres grupos principales: metales, no metales y metaloides (semi-metales). Otras agrupaciones elementales incluyen metales alcalinos, halógenos y gases nobles.[2]
2 Encuentra tu elemento en la tabla periódica. La tabla ordena elementos por número atómico y los separa en tres grupos principales: metales, no metales y metaloides (semi-metales). Otras agrupaciones elementales incluyen metales alcalinos, halógenos y gases nobles.[2] - Usar el grupo (columnas) o el período (filas) puede hacer que el elemento sea más fácil de ubicar en la tabla.
- También puede buscar el símbolo del elemento en la tabla si no conoce otras propiedades.
-
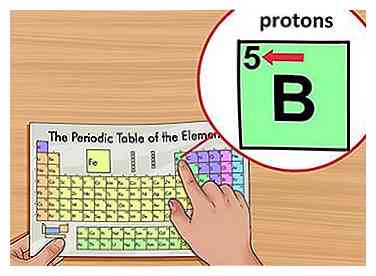 3 Ubica el número atómico del elemento. El número atómico está ubicado sobre el símbolo del elemento, en la esquina superior izquierda del cuadrado. El número atómico te dirá cuántos protones componen un solo átomo de un elemento.[3]
3 Ubica el número atómico del elemento. El número atómico está ubicado sobre el símbolo del elemento, en la esquina superior izquierda del cuadrado. El número atómico te dirá cuántos protones componen un solo átomo de un elemento.[3] - Por ejemplo, el boro (B) tiene un número atómico de 5, por lo tanto, tiene 5 protones.
-
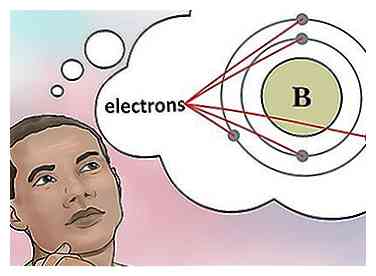 4 Determine la cantidad de electrones. Los protones son partículas en el núcleo de un átomo que tienen una carga positiva igual a +1. Los electrones son partículas que tienen una carga negativa igual a -1. Por lo tanto, un elemento en un estado neutral tendrá la misma cantidad de protones y electrones.
4 Determine la cantidad de electrones. Los protones son partículas en el núcleo de un átomo que tienen una carga positiva igual a +1. Los electrones son partículas que tienen una carga negativa igual a -1. Por lo tanto, un elemento en un estado neutral tendrá la misma cantidad de protones y electrones. - Por ejemplo, el boro (B) tiene un número atómico de 5, por lo tanto, tiene 5 protones y 5 electrones.
- Sin embargo, si el elemento incluye un ion negativo o positivo, entonces los protones y los electrones no serán los mismos. Tendrás que calcularlos. El número de ion aparecerá como un pequeño superíndice después del elemento.
-
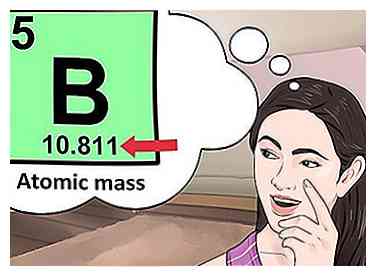 5 Busque la masa atómica del elemento. Para encontrar la cantidad de neutrones, primero deberá encontrar la masa atómica. La masa atómica de un elemento (también conocida como peso atómico) es la masa promedio ponderada de los átomos de un elemento.[4] La masa atómica se puede encontrar debajo del símbolo del elemento.
5 Busque la masa atómica del elemento. Para encontrar la cantidad de neutrones, primero deberá encontrar la masa atómica. La masa atómica de un elemento (también conocida como peso atómico) es la masa promedio ponderada de los átomos de un elemento.[4] La masa atómica se puede encontrar debajo del símbolo del elemento. - Asegúrese de redondear la masa atómica al número entero más cercano. Por ejemplo, la masa atómica de boro es 10.811, pero puede redondear la masa atómica hasta 11.
-
 6 Reste el número atómico de la masa atómica. Para encontrar la cantidad de neutrones, deberá restar el número atómico de la masa atómica. Recuerde que el número atómico es el mismo que el número de protones que ya ha identificado.[5]
6 Reste el número atómico de la masa atómica. Para encontrar la cantidad de neutrones, deberá restar el número atómico de la masa atómica. Recuerde que el número atómico es el mismo que el número de protones que ya ha identificado.[5] - Para nuestro ejemplo de boro, 11 (masa atómica) - 5 (número atómico) = 6 neutrones
Parte dos de dos:
Cálculo de los electrones con presencia de iones
-
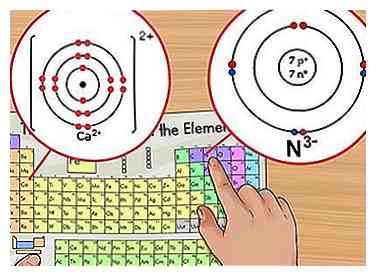 1 Identifica la carga neta. La carga neta de un ion aparecerá como un pequeño número superíndice después del elemento. Un ion es un átomo que tiene una carga positiva o negativa debido a la adición o eliminación de electrones.[6] Aunque el número de protones en el átomo sigue siendo el mismo, la cantidad de electrones se altera en un ion.
1 Identifica la carga neta. La carga neta de un ion aparecerá como un pequeño número superíndice después del elemento. Un ion es un átomo que tiene una carga positiva o negativa debido a la adición o eliminación de electrones.[6] Aunque el número de protones en el átomo sigue siendo el mismo, la cantidad de electrones se altera en un ion. - Debido a que un electrón tiene una carga negativa, cuando eliminas los electrones, el ion se vuelve positivo. Cuando agregas más electrones, el ion se vuelve negativo.
- Por ejemplo, N3- tiene una carga de -3 mientras Ca2+ tiene una carga +2.
- Tenga en cuenta que no tiene que hacer este cálculo si no hay un número de ion superpuesto después del elemento.
-
 2 Reste la carga del número atómico. Cuando un ion tiene una carga positiva, el átomo ha perdido electrones. Para calcular la cantidad restante de electrones, resta la cantidad de carga extra del número atómico. En el caso de un ion positivo, hay más protones que electrones.
2 Reste la carga del número atómico. Cuando un ion tiene una carga positiva, el átomo ha perdido electrones. Para calcular la cantidad restante de electrones, resta la cantidad de carga extra del número atómico. En el caso de un ion positivo, hay más protones que electrones. - Por ejemplo, Ca2+ tiene una carga +2 por lo que ha perdido 2 electrones desde el estado neutral. El número atómico del calcio es 20, por lo tanto, el ion tiene 18 electrones.
-
 3 Agregue la carga al número atómico para iones negativos. Cuando un ion tiene una carga negativa, el átomo ha ganado electrones. Para calcular la cantidad total de electrones presentes, simplemente agrega la cantidad de carga extra al número atómico. En el caso de un ion negativo, hay menos protones que electrones.
3 Agregue la carga al número atómico para iones negativos. Cuando un ion tiene una carga negativa, el átomo ha ganado electrones. Para calcular la cantidad total de electrones presentes, simplemente agrega la cantidad de carga extra al número atómico. En el caso de un ion negativo, hay menos protones que electrones. - Por ejemplo, N3- tiene una carga de -3; por lo tanto, ha ganado 3 electrones en comparación con el estado neutral. El número atómico de nitrógeno es 7, por lo tanto, este ion tiene 10 electrones.
Facebook
Twitter
Google+
 Minotauromaquia
Minotauromaquia
 1 Obtenga una tabla periódica de elementos. La tabla periódica es una tabla que organiza elementos por su estructura atómica. Está codificado por colores y le asigna a cada elemento una abreviatura única de 1 o 2 letras. Otra información elemental incluye el peso atómico y el número atómico.[1]
1 Obtenga una tabla periódica de elementos. La tabla periódica es una tabla que organiza elementos por su estructura atómica. Está codificado por colores y le asigna a cada elemento una abreviatura única de 1 o 2 letras. Otra información elemental incluye el peso atómico y el número atómico.[1]  2 Encuentra tu elemento en la tabla periódica. La tabla ordena elementos por número atómico y los separa en tres grupos principales: metales, no metales y metaloides (semi-metales). Otras agrupaciones elementales incluyen metales alcalinos, halógenos y gases nobles.[2]
2 Encuentra tu elemento en la tabla periódica. La tabla ordena elementos por número atómico y los separa en tres grupos principales: metales, no metales y metaloides (semi-metales). Otras agrupaciones elementales incluyen metales alcalinos, halógenos y gases nobles.[2]  3 Ubica el número atómico del elemento. El número atómico está ubicado sobre el símbolo del elemento, en la esquina superior izquierda del cuadrado. El número atómico te dirá cuántos protones componen un solo átomo de un elemento.[3]
3 Ubica el número atómico del elemento. El número atómico está ubicado sobre el símbolo del elemento, en la esquina superior izquierda del cuadrado. El número atómico te dirá cuántos protones componen un solo átomo de un elemento.[3]  4 Determine la cantidad de electrones. Los protones son partículas en el núcleo de un átomo que tienen una carga positiva igual a +1. Los electrones son partículas que tienen una carga negativa igual a -1. Por lo tanto, un elemento en un estado neutral tendrá la misma cantidad de protones y electrones.
4 Determine la cantidad de electrones. Los protones son partículas en el núcleo de un átomo que tienen una carga positiva igual a +1. Los electrones son partículas que tienen una carga negativa igual a -1. Por lo tanto, un elemento en un estado neutral tendrá la misma cantidad de protones y electrones. 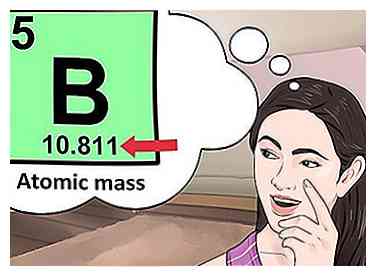 5 Busque la masa atómica del elemento. Para encontrar la cantidad de neutrones, primero deberá encontrar la masa atómica. La masa atómica de un elemento (también conocida como peso atómico) es la masa promedio ponderada de los átomos de un elemento.[4] La masa atómica se puede encontrar debajo del símbolo del elemento.
5 Busque la masa atómica del elemento. Para encontrar la cantidad de neutrones, primero deberá encontrar la masa atómica. La masa atómica de un elemento (también conocida como peso atómico) es la masa promedio ponderada de los átomos de un elemento.[4] La masa atómica se puede encontrar debajo del símbolo del elemento.  6 Reste el número atómico de la masa atómica. Para encontrar la cantidad de neutrones, deberá restar el número atómico de la masa atómica. Recuerde que el número atómico es el mismo que el número de protones que ya ha identificado.[5]
6 Reste el número atómico de la masa atómica. Para encontrar la cantidad de neutrones, deberá restar el número atómico de la masa atómica. Recuerde que el número atómico es el mismo que el número de protones que ya ha identificado.[5]  1 Identifica la carga neta. La carga neta de un ion aparecerá como un pequeño número superíndice después del elemento. Un ion es un átomo que tiene una carga positiva o negativa debido a la adición o eliminación de electrones.[6] Aunque el número de protones en el átomo sigue siendo el mismo, la cantidad de electrones se altera en un ion.
1 Identifica la carga neta. La carga neta de un ion aparecerá como un pequeño número superíndice después del elemento. Un ion es un átomo que tiene una carga positiva o negativa debido a la adición o eliminación de electrones.[6] Aunque el número de protones en el átomo sigue siendo el mismo, la cantidad de electrones se altera en un ion.  2 Reste la carga del número atómico. Cuando un ion tiene una carga positiva, el átomo ha perdido electrones. Para calcular la cantidad restante de electrones, resta la cantidad de carga extra del número atómico. En el caso de un ion positivo, hay más protones que electrones.
2 Reste la carga del número atómico. Cuando un ion tiene una carga positiva, el átomo ha perdido electrones. Para calcular la cantidad restante de electrones, resta la cantidad de carga extra del número atómico. En el caso de un ion positivo, hay más protones que electrones.  3 Agregue la carga al número atómico para iones negativos. Cuando un ion tiene una carga negativa, el átomo ha ganado electrones. Para calcular la cantidad total de electrones presentes, simplemente agrega la cantidad de carga extra al número atómico. En el caso de un ion negativo, hay menos protones que electrones.
3 Agregue la carga al número atómico para iones negativos. Cuando un ion tiene una carga negativa, el átomo ha ganado electrones. Para calcular la cantidad total de electrones presentes, simplemente agrega la cantidad de carga extra al número atómico. En el caso de un ion negativo, hay menos protones que electrones.